第二节 分子结构
所谓分子结构通常包括下面一些内容:分子中直接相邻的原子间的强相互作用力,即化学键问题,分子的空间构型问题;分子之间还有一种弱的相互作用力,即分子间力问题;此外分子间或分子内的一些原子间还可能形成氢键。
本节主要简介杂化轨道理论,有关氢键的问题留在下一节讨论。
一、化学键的概念
分子或晶体中相邻原子间强烈的相互作用力称为化学键。化学键的基本类型有:离子键(电价键)、共价键、配价键和金属键等。
以阳离子和阴离子之间静电引力形成的化学键 叫离子 键。
分子中原子间通过共享电子对所形成的化学键为共价键。
配价键是一种特殊的共价键,其共享电子对是一个原子单独提供的。这种由一个原子单独提供一对电子与另一个原子共享所形成的共价键,叫配位共价键,简称配价键。
自1916年刘易斯提出经典的共价键理论以来,共价键理论有了很大的发展。现代共价键理论有两种,一是价键理论,二是分子轨道理论。本书不介绍轨道理论。
(一)价键理论的基本要点
价键理论,又称电子配对法,其基本要点如下:
1.具有自旋相反的未成对电子的两个原子相互接近,可以形成稳定的共价键。
如果A、B两个原子各有一个自旋相反的未成对的电子,那么这两个未成对电子可以相互配对形成稳定的共价键,这对电子为A、B两原子所共有。如果A、B各有两个或三个未成对的电子,则自旋相反的单电子可两两配对形成共价键或叁键。
如果A原子有两个未成对电子,B原子有一个未成对电子,那么一个A原子能与两个B原子结合形成AB2型分子。
2.原子中未成对的电子数等于原子所能形成的共价键数目。
共价键是由成键原子中自旋相反的未成对电子配对形成的。一个原子的一个电子和另一个原子的一个电子配对以后,不能再和第二个电子配对。因为这时其中必有两个电子的自旋方向相同而相斥。也就是说一个原子所能形成共价键的数目是一定的。原子中未成对的电子数等于原子所能形成的共价键数目,这就是共键价的饱和性。例如,H原子只有一个未成对电子,它和另一个H原子的未成对电子配对后,就不能再与第二个H原子的电子配对了。
3.成键电子的电子云重叠越多,核间电子子云密度越大,形成的共价键越牢固。
共价键的生成是由于自旋相反的单电子相互配对,电子云重叠的结果。因此,当两个原子形成分子时,电子云重叠的程度越大,则两原子间的电子云密度越大,生成的共价键越牢固,所以,在形成共价键时,电子云总是尽可能达到晨大程度的重叠,这叫电子云最大重叠原理。
根据电子云最大重叠原理,在形成共价键时,原子间总是尽可能沿着电子云最大重叠方向成键。s电子云呈球形对称分布,p、d、f电子云在空间都有一定的伸展方向。在形成共价键时,除了s电子云和s电子云可以在任何方向上都能达到最大程度的重叠外,p、d电子云的重叠,只有在一定方向上才能使电子云有最大程度的重叠。即共价键是有方向性的。例如,当氢原子1s电子云和氯原子的3p电子云重叠形成HCL分子时,氢原子的1s电子云总是沿着氯原子未成对电子的3p电子云对称轴方向作最大程度的重叠(图4-9(a))。其他方向都不能形成稳定的分子(图4-9(b)(c))。
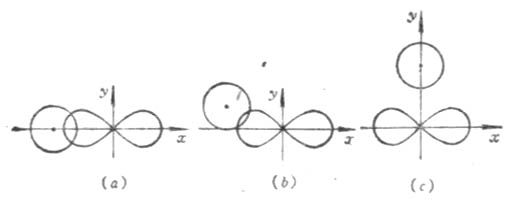
图4-9 氢原子的1s电子云与氧原子的3P[XB]χ[/XB]电子云的三种重叠情况
(二)共价键的类型
共价键有两种成键方式。一种是电子云以:“头碰头”方式相重叠,电子云及重叠部分沿键轴(两核间连线)呈圆柱形对称分布,重叠部分绕轴旋转任何角度形状不会改变,这种键叫σ键。另一种是成键的两个电子云的对称轴相平行,以“肩并肩”方式相重叠,电子云重叠部分对通过键轴的一个平面具有对称性,这种键称为π键。
例如在N2分子中,氮原子的电子层结构为1s22s22p1x2p1y2p1z三个未成对的p电子分占三个互相垂直的p轨道。当两个氮原子结合成N2分子时,px电子云沿x轴方向以“头碰头”方式重叠形成一个σ键,每个原子剩下的两个p电子云不能再沿x轴方向“头碰头”重叠,只能让p电子云的对称轴平行,以“肩并肩”方式重叠形成两个π键。如图4-10。
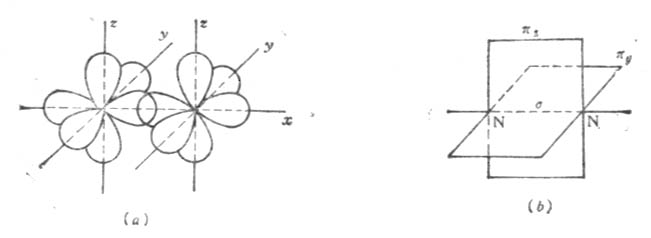
图4-10 N2分子形成示意图
由于σ键电子云重叠程度较π键大,因而σ键比π键牢固。一般来说,π键容易断开,化学活泼性较强。π键不能单独存在,只能与σ键共存于具有双键或叁键的分子中。σ键不易断开,是构成分子的骨架,可单独存在于两原子间。通常在以共价键结合的两原子间只能有一个σ键。
二、杂化轨道理论
价键理论比较简明地阐明了共价键的本质,共价键的饱和性和方向性。但在解释分子的空间结构方面却遇到了困难。例如,经实验测知,甲烷分子具有正四面体的空间构型,如图4-11所示。图中实线代表C-H键,虚线表示CH4分子具有正四面体的空间构型。碳原子位于四面体的中心,与四个氢原子形成四个等同的C-H键,指向四面体的顶点,两个C-H键间夹角(<HCH)为109°28’。
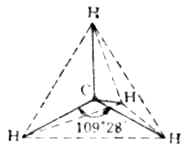
图4-11 CH[XB]4[/XB]分子构型
碳原子的外层电子构型是2s22p1x2p1y有两个未成对的p电子,按照价键理论,碳只能与两个氢原子形成两个共价键。如果考虑将碳原子的一个2s电子激发到2p空轨道上去,则碳原子有四个未成对电子(一个s电子和三个p电子),可与四个氢原子的1s电子配对形成四个C-H键。从能量观点上看,2s电子激发到2p轨道所需要的能量(402kJ·mol-1)可能被多形成两个C-H键所放出的能量(410KJ.mol-1)所补偿而余。由于碳原子的2s电子和2p电子的能量不同,形成的四个C-H键也应当不同,这与实验事实不符。为了解决这个矛盾,1931年鲍林(Pauling)和斯莱脱(Slater)提出了杂化轨道理论,进一步发展和丰富了现代价键理论。

(一)杂化轨道理论的基本要要点
1.在成键过程中,由于原子间的相互影响,同一原子中参加成键的几个能量相近的原子轨道可以进行混合,重新分配能量和空间方向,组成数目相等的新原子轨道。这种轨道重新组合的过程称为轨道杂化,简称杂化。所组成的新原子轨道叫做杂化轨道。
2.杂化轨道之间互相排斥,力图在空间取得最大的键角,使体系能量降低。原子轨道杂化以后所形成的杂化轨道更有利于成键。因为杂化后原子轨道的开头发生了变化,如s轨道和p轨道杂化形成的杂化轨道,使本来平分在对称两个方向上的p轨道比较集中在一个方向上,变成一头大一头小,成键时在较大一头重叠,有利于最大重叠。因此杂化轨道的成键能力比单纯轨道的成键能力强。
(二)杂化轨道类型
根据原子轨道的种类和数目不同,可以组成不同类型的杂化轨道。这里我们只介绍s轨道和p轨道之间的杂化。
1.Sp杂化
一个s轨道和一个p轨道杂化可组成两个sp杂化轨道。每个sp杂化轨道各含有1/2s和1/2p成分。两个杂化轨道夹角为180°。
两个sp杂化轨道的对称轴在同一条直线上,只是方向相反(图4-12)。因此sp杂化轨道又叫直线形杂化轨道。
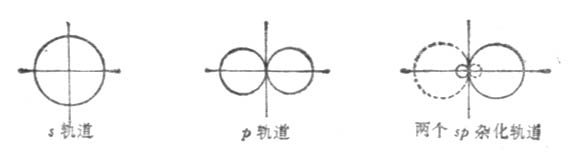
图 4-12 sp杂化轨道的形成
气态BeCL2是直线形分子,铍原子的电子层结构为1s22s2,似乎不会形成共价键。但实际上铍可与氯气反应生成BeCL2共价分子。根据杂化轨道理论,铍原子成键时,2s轨道上的一个电子先被激发到一个空的2p轨道上去,然后由含有一个未成对电子的2s轨道和2p轨道进行sp杂化形成能量相等夹角为180°的两个sp杂化轨道。两个杂化轨道再分别与两个氯原子的3p轨道重叠,形成两个互为180°的Be-Cl键,它们是(sp-p)σ键。因此BeCL2是直线形分子(图4-13)。
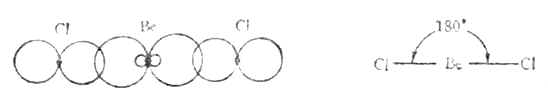
图4-13 BeCL2分子型
2.sp2杂化
一个s轨道和两个p轨道杂化可组成三个sp2杂化轨道。每个sp2杂化轨道有1/3s成分,2/3p成分。两个sp2杂化轨道间的夹角120°。
三个sp2杂化轨道的取向是指向平面三角形的三个顶角,因此sp2杂化轨道又叫平面三角形杂化轨道(图4-14)。

图4-14 三个sp[SB]2[/SB]杂化轨道
BF3是平面三角形分子。硼原子的价电子结构为2s22p1。当硼与氟反应时,硼原子2s轨道上的一个电子先激发到空的2p轨道上去,然后一个2s轨道和两个2p轨道进行sp2杂化形成三个夹角为120°的sp2杂化轨道。每个sp2杂化轨道与F原子的一个2p轨道重叠组成一个(sp2-p)σ键。BG3是平面三角形结构。分子中四个原子处在同一平面上,B原子位于中心(图4-15)。
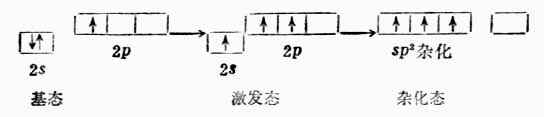
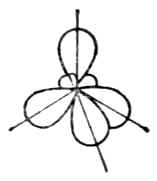
图4-15 BF分子构成 图4-16四个sp杂化轨道
3.sp3杂化
一个s轨道和三个p轨道杂化形成四个sp3杂化轨道,每个sp3杂化轨道含有1/4s和3/4p成分。每两个杂化轨道间的夹角为109°28’。
四个sp3杂化轨道的取向是指向正四面体的四个顶角。所以sp3杂化轨道也称正四面体杂化轨道(图4-16)。
在形成CH4分子时,碳原子的一个2s电子先激发到空的2p轨道上去然后一个2s轨道和三个2p轨道杂化组成四个等同的sp3杂化轨道。四个氢原子的1s轨道分别同碳原子的四个sp3杂化轨道重叠,组成四个(sp3-p)σ键,形成CH4分子。
